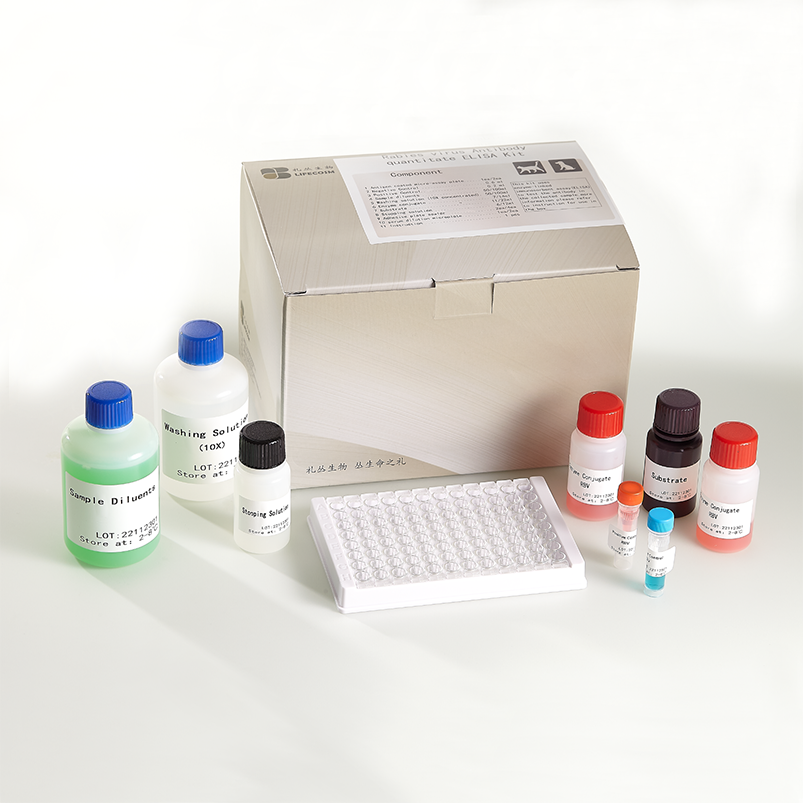
สินค้า
ชุดตรวจ Elisa ไวรัสโรคติดเชื้อในถุงน้ำในไก่
ชุดตรวจ Elisa ไวรัสโรคติดเชื้อในถุงน้ำในไก่
| สรุป | การตรวจหาแอนติบอดีที่เป็นกลางต่อถุงน้ำที่ติดเชื้อของไวรัส Fabricius ในซีรั่มไก่ |
| เป้าหมายการตรวจจับ | แอนติบอดีไวรัสโรคถุงน้ำในไก่ |
| ตัวอย่าง | เซรั่ม
|
| ปริมาณ | 1 ชุด = ทดสอบ 192 ครั้ง |
|
ความเสถียรและการเก็บรักษา | 1) ควรเก็บสารเคมีทั้งหมดไว้ที่อุณหภูมิ 2~8℃ ห้ามแช่แข็ง 2) อายุการใช้งาน 12 เดือน ใช้สารเคมีให้หมดก่อนวันหมดอายุที่ระบุบนชุดทดสอบ
|
ข้อมูล
โรคถุงน้ำในตาติดเชื้อ(IBD) หรือที่รู้จักกันในชื่อโรคกัมโบโร โรคเยื่อบุข้ออักเสบติดเชื้อ และโรคไตอักเสบในนกติดเชื้อ เป็นโรคติดต่อร้ายแรงในเด็กเล็กไก่และไก่งวงที่เกิดจากไวรัสโรคเยื่อบุข้ออักเสบติดเชื้อ (IBDV) ซึ่งมีลักษณะดังนี้ภูมิคุ้มกันบกพร่องและอัตราการเสียชีวิตโดยทั่วไปจะอยู่ที่อายุ 3 ถึง 6 สัปดาห์ โรคนี้ถูกค้นพบครั้งแรกในกัมโบโร เดลาแวร์ในปีพ.ศ. 2505 ถือเป็นเรื่องสำคัญทางเศรษฐกิจต่ออุตสาหกรรมสัตว์ปีกทั่วโลก เนื่องจากมีความเสี่ยงต่อโรคอื่นๆ เพิ่มมากขึ้น และยังมีผลกระทบเชิงลบต่อประสิทธิภาพการฉีดวัคซีนในช่วงไม่กี่ปีที่ผ่านมา ไวรัส IBDV สายพันธุ์ที่ก่อโรคร้ายแรง (vvIBDV) ซึ่งทำให้ไก่ตายเป็นจำนวนมาก ได้แพร่ระบาดในยุโรปละตินอเมริกา-เอเชียตะวันออกเฉียงใต้, แอฟริกาและตะวันออกกลางการติดเชื้อเกิดขึ้นผ่านทางอุจจาระในปาก โดยไก่ที่ติดเชื้อจะขับถ่ายไวรัสออกมาในปริมาณสูงเป็นเวลาประมาณ 2 สัปดาห์หลังจากติดเชื้อ โรคนี้แพร่กระจายได้ง่ายจากไก่ที่ติดเชื้อไปยังไก่ที่แข็งแรงผ่านอาหาร น้ำ และการสัมผัสทางกายภาพ
หลักการของการทดสอบ
ชุดทดสอบใช้การทดสอบ ELISA แบบแข่งขัน โปรตีน VP2 ของไวรัสโรคถุงน้ำติดเชื้อที่บรรจุไว้ล่วงหน้าบนไมโครเพลท และแข่งขันกับแอนติบอดีต่อโปรตีน VP2 ในซีรั่มสำหรับเวกเตอร์เฟสแข็งโดยใช้แอนติบอดีโมโนโคลนอลต่อโปรตีน VP2 ในการทดสอบ แอนติบอดีโมโนโคลนอลที่จะทดสอบและโปรตีน VP2 จะถูกเติมลงไป และหลังจากฟัก หากตัวอย่างมีแอนติบอดีเฉพาะโปรตีน VP2 ของไวรัสโรคถุงน้ำติดเชื้อในไก่ แอนติบอดีจะจับกับแอนติเจนบนเพลทเคลือบ จึงปิดกั้นการจับกันของแอนติบอดีโมโนโคลนอลต่อโปรตีน VP2 กับแอนติเจน หลังจากล้างเพื่อกำจัดแอนติบอดีที่ไม่จับกับส่วนประกอบอื่นๆ จากนั้นจึงเติมแอนติบอดีรองที่ติดฉลากเอนไซม์ของเมาส์เพื่อจับกับคอมเพล็กซ์แอนติเจน-แอนติบอดีบนเพลทตรวจจับโดยเฉพาะ คอนจูเกตเอนไซม์ที่ไม่จับกับแอนติบอดีจะถูกกำจัดออกโดยการล้าง เติมสารตั้งต้น TMB ลงในไมโครเวลล์เพื่อพัฒนาสี และค่าการดูดกลืนแสงของตัวอย่างมีความสัมพันธ์เชิงลบกับเนื้อหาของแอนติบอดีต่อโปรตีน VP2 ที่มีอยู่ภายใน จึงบรรลุวัตถุประสงค์ในการตรวจจับแอนติบอดีต่อโปรตีน VP2 ในตัวอย่าง
เนื้อหา
| สารเคมี | ปริมาณ 96 ทดสอบ/192ทดสอบ | ||
| 1 |
| 1อัน/2อัน | |
| 2 |
| 2.0มล. | |
| 3 |
| 1.6มล. | |
| 4 |
| 100มล. | |
| 5 |
| 100มล. | |
| 6 |
| 11/22มล. | |
| 7 |
| 11/22มล. | |
| 8 |
| 15มล. | |
| 9 |
| 2ตัว/4ตัว | |
| 10 | ไมโครเพลทเจือจางซีรั่ม | 1อัน/2อัน | |
| 11 | คำแนะนำ | 1 ชิ้น |